产品分类
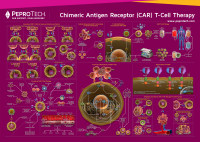
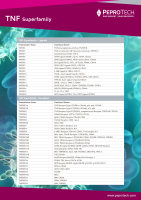
精美挂图(poster)
联系方式
- 公司地址
-
上海市浦东新区金桥路27号
邮编:
- 联系电话
- 4008****82登录查看商家电话
- 传真号码
- 电子邮箱
- peprotech.infochina@****mofisher.com登录查看商家邮箱
- 公司网址
- www.peprotech.com
公司新闻
PeproTech助力肌萎缩性侧索硬化(ALS)研究!
发布时间:2017-05-19 14:11 | 点击次数:
| PeproTech助力肌萎缩性侧索硬化(ALS)研究 |
| 近几天朋友圈被一则消息刷屏。BrainStorm Cell Therapeutics公司在英国国际伦敦国际细胞治疗学会(ISCT)年会以及世界先进疗法和再生医学大会上公布NurOwn®治疗肌萎缩性侧索硬化ALS的II期临床研究数据,结果良好……渐冻人解冻有望! |
何为渐冻人 |
| 2014年夏天的冰桶挑战活动,吸引了奥巴马、比尔盖茨等政界、商界、娱乐界领袖纷纷参与,风靡全球,大多数人是因为这个活动才开始了解渐冻症。 渐冻症医学上称为ALS,就是肌肉萎缩性侧索硬化症。 这是一种侵犯大脑和脊髓中神经元的进行性神经退行性疾病。ALS患者的运动神经元细胞不断衰亡,最终会失去控制肌肉活动的能力,导致完全瘫痪或死亡。霍金所患的疾病就是渐冻人症中罕见的一种亚型。 
|
为何ALS此临床II期的结果如此轰动 |
| 由于渐冻症神经细胞死亡的原因不清,所以新药研发比较困难,目前尚无有效药物可以阻止或者逆转疾病的进行。很多人寄希望于干细胞疗法,希望可以通过修复损伤的神经元治疗该病,改善患者的生存质量。 而此次公布的二期临床结果显示,接受NurOwn®干细胞疗法的很多患者,不同症状有了不同程度的改善,这无疑给患者及其家人带来了极大的希望。 |
什么是NurOwn®技术 |
| NurOwn®技术是在特拉维夫大学教授Dani Offen教授和已故教授Eldad Melamed的实验室开发的,已发表多篇文献。Brainstorm cell Therapeutics通过技术转让协议拥有了NurOwn技术的开发和商业化权利。 NurOwn®技术的关键在于将MSC诱导成MSC-NTF细胞的过程。MSC-NTF可以分泌各种神经营养因子,包括胶质衍生神经营养因子(GDNF),脑源性神经营养因子(BDNF),血管内皮生长因子(VEGF)和肝细胞生长因子(HGF)。 该细胞可以保护神经元免受毒素影响,并且在ALS,坐骨神经损伤,帕金森病,多发性硬化,视神经缺血和亨廷顿疾病的动物模型中都有效。 
MSC-NTF细胞是从已经在体外扩增和分化的自体骨髓来源的MSC产生的。从患者体内抽出脊髓。分离MSC培养2-3周。MSC可以直接制成MSC-NTF细胞,或者冷冻储存以备将来使用。 将MSC转化为MSC-NTF细胞的过程大约需要6天。细胞在专利条件下生长,被诱导分泌更高水平的神经营养因子。收获细胞,患者给药。 |
我们产品的助力 |
| 细胞治疗良好的安全性和细胞培养息息相关,NurOwn®技术,细胞的整个生产过程不使用动物来源的产品,如胎牛血清,也不会在生产过程中使用抗生素。 我们都知道在干细胞培养中细胞因子扮演了重要的角色,而BrainStorm生产中使用的细胞因子如,FGF-basic等均来自PeproTech AF级别细胞因子,即animal free级别细胞因子。 出色的产品才能助力出色的科研,出色的科研成果与人类健康和生存息息相关。 干细胞疗法作为一种有效的极具前景的疗法,近年来得到越来越多的关注,也获得了许多激动人心的结果,希望在优质产品的助力下,相关的研究可以成功完成科研-临床的转化,最终改善人类生存质量。 |
BrainStorm临床研究及市场 |

临床1/2期研究在Hadassah医学中心进行。研究的结果在2013年美国神经病学研究所提出。 IT组由晚期患者组成,IM组由早期受试者组成。无严重的不良事件与MSC-NTF细胞给药相关。IT组的受试者,治疗后6个月较治疗3个月相比,ALS功能表评分的结果显示,进展速度显着改善。与预期进展时间相比,两组患者在治疗后的进展率较低。 临床2a期研究在Hadassah医学中心进行。研究的结果在2015年美国神经病学研究所提出。 一项剂量升级、单臂临床2a期试验在该中心进行。共有14名早期ALS患者参加,分为三个剂量组(低剂量,中剂量和高剂量),单次给予IT和IM两种MSC-NTF细胞。无严重的不良事件与MSC-NTF的施用相关联,并且在1/2期试验中,绝大多数观察到的不良事件均为I-II级短暂性事件。本研究中的受试者在治疗后6个月也显示ALS功能表评分和FVC进展与三个月期间相比速度明显改善。 |
ALS在美国的临床试验 |
| 这次II期临床是在美国3个中心开展:麻省总医院、麻省大学医学院和梅奥诊所进行。该研究是一项多中心,随机,双盲,安慰剂对照的ALS临床试验,招募了48名早期ALS患者,随机化3:1接受治疗与安慰剂。 旨在评价单次NurOwn治疗48例ALS患者的效果,以安全性和耐受性为主要终点,以ALS功能量表评分、生物标记物等为次要终点。这项研究的首选结果于2016年7月18日发布。治疗组36例、安慰剂组12例,一次治疗后随访观察6个月。 第12周时治疗组40%的患者实现50%以上改善,而安慰剂组只有17%的患者实现50%以上改善。即使从其他多个维度来看,接受该疗法显著获益。 
|
| 2017年3月BrainStorm和再生药物商业化中心(CCRM)签署了一项协议以支持他ALS疗法的上市许可要求。CCRM也正帮助BrainStorm寻找获得加拿大卫生部早期使用途径治疗ALS患者的机会,加速向市场产品的转化。 总之,整个临床结果还是非常鼓舞的,对于渐冻人来说就是解冻的曙光,希望可以顺利三期,推向临床,给患者带来真正的福音。 |
| PeproTech(派普泰克)中国代表处 江苏省苏州市玉山路99号钻石广场2幢416室 邮编:215011 电话:0512-6832 5983/6832 5993 企业qq:800053055(在线咨询) Email:china@peprotech.com Website:www.peprotech.com |